практические (творческие задания).
портреты ученых.
реактивы: серная кислота, сахарная пудра, перманганат калия, порошок угля, порошок железа, порошок магния, вода;
посуда: воронка, фильтр, химические стаканы, тигель, штатив, стеклянная палочка.
| № п/п | Этапы урока | Деятельность учителя | Деятельность учащихся |
| 1 | Организационный момент | Приветствие | Приветствие |
| 2. | Актуализация знаний учащихся Проблемное задание | - Прослушайте стихотворение и определите тему сегодняшнего урока: Эта память – верьте, люди, -
Всей земле нужна.
Если мы войну забудем, -
Вновь придёт война! Какая тема урока? - Как вы думаете, почему мы начали урок именно с этих слов? Кто знает автора этих строк? | -Великая Отечественная война и химия. -Автор этих строк Роберт Рождественский. -Эти строки указывают нам, что все мы, ныне живущие, обязаны помнить о тех страшных военных годах, и о том, какой ценой завоевана наша мирная жизнь.
|
| 3 | Введение новых знаний
| Ребята, к нам в руки попали архивные документы, но так как со дня Победы прошло … Сколько лет?
| 80 лет |
| Верно. Документы немного испортились, и наша с вами сегодня задача восстановить потерянную информацию. На экран через проектор проецирует бутылку с надписью «КС» и уравнения реакций KClO3 + H2SO4 = ClO2 + KСlO4 + K2SO4 + H2O, ClO2 = Cl2 + O2, C12H22O11 + O2 = CO2 + H2O. -Как вы думаете, что означает надпись «КС» и уравнения реакций? | Это бутылка с зажигательной смесью Качурина – Солодовника и реакции, иллюстрирующие действие запала |
| Прослушивание сообщений учащихся | Как по - другому называют эту горючую смесь и что вы о ней знаете из дополнительных источников? | -Коктейль Молотова. - Вспомним начало войны, 1941 г. Немецкие танки рвались к Москве, Красная Армия буквально грудью сдерживала врага. Не хватало обмундирования, продовольствия и боеприпасов, но самое главное – катастрофически не хватало противотанковых средств. В этот критический период на помощь пришли ученые-энтузиасты: в два дня на одном из военных заводов был налажен выпуск бутылок КС (Качурина–Солодовника), или просто бутылок с горючей смесью. Это незамысловатое химическое устройство уничтожало немецкую технику не только в начале войны, но и даже весной 1945г. в Берлине.
|
| Что представляли собой бутылки КС? | К обыкновенной бутылке прикреплялись резинкой ампулы, содержащие концентрированную серную кислоту, бертолетову соль, сахарную пудру. В бутылку заливали бензин, керосин или масло. Как только такая бутылка при ударе разбивалась о броню, компоненты запала вступали в химическую реакцию, происходила сильная вспышка, и горючее воспламенялось. Три компонента запала берутся в отдельности, их нельзя смешивать заранее, т.к. получается взрывоопасная смесь.
|
| Работа с уравнениями реакций | Расставьте коэффициенты в данных уравнениях реакций | 3KClO3 + H2SO4 = 2ClO2 + KСlO4 + K2SO4 + H2O, 2ClO2 = Cl2 + 2O2, C12H22O11 + 12O2 = 12CO2 +11 H2O.
|
| Прослушивание сообщения учителя. | Было бы не справедливо не вспомнить сегодня о порохе. В основном во время войны использовался нитроцеллюлозный (бездымный) и чёрный (дымный) порох. Грозные боевые машины тех лет - легендарная "катюша", знаменитый штурмовик ИЛ-2 были вооружены реактивными снарядами, топливом для которых служили бездымные пороха. | В состав черного пороха входит нитрат калия, найдите массовую долю калия в нитрате калия. Работают в парах. |
| Прослушивание сообщений учащихся | А какие химические изобретения известны вам со времен Великой Отечественной войны? | Многие наши сверстники в военные годы во время налетов дежурили на крышах домов, тушили зажигательные бомбы. Начинкой таких бомб была смесь порошков Al, Mg и оксида железа, детонатором служила гремучая ртуть. При ударе бомбы о крышу срабатывал детонатор, воспламенявший зажигательный состав, и все вокруг начинало гореть.
|
| Работа с уравнениями реакций | На экране проецирует уравнения химических реакций, происходящие при взрыве бомбы: Al + O2 = Al2O3, Mg + O2 = MgO, Fe3O4 + Al = Fe + Al2O3. Расставьте коэффициенты в уравнениях реакций | 4Al + 3O2 = 2Al2O3, 2Mg + O2 = 2MgO, 3Fe3O4 + 8Al = 9Fe + 4Al2O3.
|
| Можно ли потушить горящий зажигательный состав водой? | Нет, так как раскаленный магний реагирует с водой: Mg + 2Н2O = Mg(ОН)2 + Н2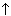 . .
|
| Демонстрационный опыт. «Взаимодействие раскаленного магния с водой». Оборудование: ложка для сжигания, плоскодонная колба на 2-3 литра, горелка, предметный столик. Реактив: порошок магния, вода.
| Плоскодонную колбу заполняю до половины водой и ставлю на предметный столик. Ложку для сжигания с порошком магния вношу в пламя горелки. Как только магний загорится, горелку убираю. Когда горение магния уменьшится, даю ему несколько охладиться и погружаю ложку в колбу с холодной водой. Каковы признаки реакции? | Происходит бурная реакция раскаленного магния с водой. Выделяющийся при этом водород загорается на поверхности воды.
|
|
| Прослушивание сообщений учащихся |
| - Во время ночных налетов для освещения бомбардировщики сбрасывали на парашютах осветительные ракеты. В состав такой ракеты входили порошок магния, спрессованный с особыми составами, и запал из угля, бертолетовой соли и солей кальция. При запуске осветительной ракеты высоко над землей красивым ярким пламенем горел запал; по мере снижения свет постепенно делался более ровным, ярким и белым – это загорался магний. Наконец, когда цель была освещена и видна так же хорошо, как и днем, летчики начинали прицельное бомбометание.
|
|
| На слайде проецирует портреты ученых-химиков, которые трудились в годы войны на победу
| Александр Ерминингельдович Арбузов. Выдающийся ученый, основоположник одного из новейших направлений науки – химии фосфорорганических соединений. Вся жизнь и деятельность его были неразрывно связаны с прославленной Казанской школой химиков. Исследования Арбузова в годы войны были всецело посвящены нуждам обороны и медицины. - Николай Дмитриевич Зелинский. В период 1941–1945 гг. – это не просто химик-исследователь, он был уже славой едва ли не самой большой в стране научной школы, исследования которой были направлены на разработку способов получения высокооктанового топлива для авиации, мономеров для синтетического каучука. - Семен Исаакович Вольфкович. Крупнейший советский химик-технолог, был директором НИИ удобрений и инсектицидов, занимался соединениями фосфора. Сотрудники руководимого им института создавали фосфорно-серные сплавы для стеклянных бутылок, которые служили противотанковыми «бомбами», изготавливали химические грелки, которые использовались для обогрева бойцов дозоров. Санитарной службе требовались средства против обморожения, ожогов, лекарственные средства.
|
|
| Минута молчания в память о погибших в годы ВОВ ученых-химиках | В память о химиках-фронтовиках было написано стихотворение бывшим фронтовиком З.И. Барсуковым:
Кто про химика сказал: “ Мало воевал”
Кто сказал: “ Он мало крови проливал?”
Я в свидетели зову химиков-друзей, –
Тех, кто смело бил врага до последних дней,
Тех, кто грудью защитил Родину мою.
Сколько пройдено дорог, фронтовых путей…
Сколько полегло на них молодых парней…
Не померкнет никогда память о войне,
Слава химикам живым, павшим – честь вдвойне. - Давайте почтим память о погибших в годы ВОВ ученых-химиках минутой молчания.
|
|
|
| Демонстрационный опыт. “Снопа” искр из тигля”: Оборудование: железный тигель, штатив с кольцом, фарфоровый треугольник, спиртовка, лист бумаги, стеклянная палочка, порошки железа и древесного угля, сухой мелкокристаллический перманганат калия | Завершаем наш урок символическим салютом в честь 75-й годовщины Великой Победы. На чистом листе бумаги (или на стекле) тщательно смешиваю стеклянной палочкой или шпателем равные количества (примерно по 1-2 чайной ложки) порошков железа, древесного угля и перманганата калия. Полученную смесь переношу в железный тигель, закрепленный в фарфоровом треугольнике, который находится на кольце штатива. Нагреваю тигель в пламени спиртовки. Через некоторое время из тигля начинают разлетаться раскаленные частички железа в виде снопа искр. |
|
| 4 | Рефлексия -размышление, рождение нового знания | Учитель возвращает учащихся к первоначальным записям-предположениям. На стадии рефлексии осуществляется анализ, творческая переработка, интерпретация изученной информации. Работа ведется в группах. Составьте синквейн по изученной теме. |
Учащиеся соотносят «новую» информацию со «старой», используя знания, полученные на уроке. |
| 5 | Домашнее задание | Подготовить презентацию «Ученые-химики в годы ВОВ» | Учащиеся записывают домашнее задание. |
















